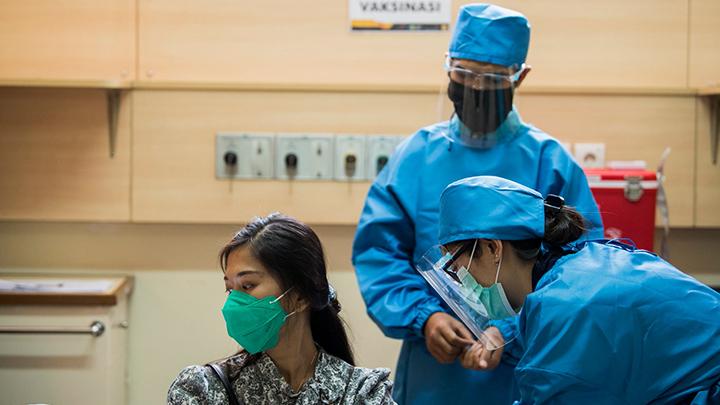
Uji Klinis Vaksin Sinovac Bermasalah di Brasil, Bio Farma Klaim Uji Coba di Indonesia Masih Aman
Berita Baru, Jakarta – Meskipun uji klinis vaksin Covid-19 produksi Sinovac mengalami masalah di Brasil. Namun, Bio Farma masih mengklaim proses uji klinis fase 3 yang dilakukan di Bandung masih berjalan aman.
Juru Bicara Tim Uji Klinis Fase 3 Vaksin Covid-19 dari Fakultas Kedokteran Universitas Padjadjaran, Rodman Tarigan, mengatakan sejauh ini belum ada laporan mengenai Kejadian Ikutan Pasca Imunisasi (KIPI) yang serius atau Serious Adverse Event (SAE), atau kejadian serius yang tidak diinginkan dari para relawan yang diduga berhubungan dengan vaksin atau kegiatan vaksinasi.
“SAE merupakan salah satu Kejadian Ikutan Pasca Imuniasi (KIPI) yang serius, yang dialami penerima obat atau vaksin, tanpa memandang hubungannya dengan obat atau vaksin tersebut,” ,” kata dia, dikutip dari rilis resmi Bio Farma, Rabu (11/11).
Sementara KIPI nonserius atau KIPI ringan, menurutnya adalah kejadian medis yang terjadi setelah imunisasi, tidak menimbulkan risiko potensial pada kesehatan penerima vaksin, seperti terjadi demam, bengkak di lokasi suntikan, atau merah di lokasi suntikan.
Lebih lanjut, anggota tim farmakovigilan dari Bio Farma, Novilia, mengatakan SAE juga bisa saja terjadi pada vaksin yang sudah dipasarkan.
“SAE yang dialami oleh seseorang, bisa terjadi baik untuk vaksin yang sudah dipasarkan, maupun vaksin yang sedang dalam tahap uji klinis seperti vaksin Covid-19 ini,” katanya.
Novilia mengatakan, untuk insiden SAE dalam fase uji klinis akan langsung dilaporkan ke Komite Etik, BPOM, dan DSMB (Data Safety Monitoring Board).
“Sedangkan untuk produk yang sudah dipasarkan akan dilakukan investigasi atau penyelidikan dan analisis oleh lembaga yang independen seperti KOMNAS KIPI, dan dilaporkan ke BPOM, untuk memastikan penyebab utama dari peristiwa ini, apakah berhubungan langsung dengan vaksin (associated to vaccine), atau ada faktor lainnya (co-incident),” terang Novilia.
SAE, misalnya, saat ini disebut-sebut sempat terjadi di Brasil pada peserta uji klinis fase 3 vaksin Covid-19 Sinovac.
“Untuk kejadian SAE yang saat ini terjadi di Brasil, perlu dilakukan investigasi lebih lanjut untuk menentukan apakah SAE ini berhubungan dengan vaksin atau bukan (co-incident). Dalam penyelidikan SAE ini, otoritas Badan Pengawas Obat setempat tentu akan dilibatkan,” kata Novilia.
Novilia mengatakan kejadian SAE bisa menangguhkan pelaksanaan uji klinis. “Jeda atau penangguhan pelaksanaan uji klinis obat atau vaksin merupakan prosedur standar dan biasa dilakukan untuk melakukan investigasi lebih dulu atas KIPI serius yang ditemukan dalam penelitian,” terangnya.
Sebelumnya, Otoritas kesehatan di Brasil membuat pengumuman mengejutkan pada Senin (09/11) malam, bahwa telah menangguhkan uji klinis vaksin Covid-19 milik Sinovac Biotech. Anvisa, otoritas itu, menyebut keputusan dibuat 29 Okober lalu setelah menemukan “efek merugikan yang parah” dari calon vaksin asal Cina tersebut.
Anvisa tidak memberikan keterangan lebih rinci tentang kasus efek samping yang dimaksud. Sebuah catatan yang menyertai perintah pembekuan uji klinis itu hanya menyebutkan agar lebih baik lagi mengevaluasi data dan mengkaji risiko.

 Rctiplus.com
Rctiplus.com pewartanusantara.com
pewartanusantara.com Jobnas.com
Jobnas.com Serikatnews.com
Serikatnews.com Serdadu.id
Serdadu.id Beritautama.co
Beritautama.co kalbarsatu.id
kalbarsatu.id surau.co
surau.co





